Содержание и последовательность изложения
Тема «Электролиз растворов и расплавов» логически продолжает изучение закономерностей протекания химических реакций, смещения равновесия обратимых процессов и является одним из существенных вопросов теории растворов. Многие вопросы промышленности, металлургии связаны с явлением гидролиза солей, поскольку он является основой их устойчивости и равновесия.
Преподавание темы «Электролиз растворов и расплавов» начинается с 9 класса, первого полугодия. При изучении этой темы пользуются учебником химии под редакцией Г. Е. Рудзитис, Ф.Г. Фельдман, также учебником за 8 - 9 класс под редакцией Н. С. Ахметова. Дидактическим материалом служит книга по химии для 8 - 9 классов под редакцией А. М. Радецкого, В. П. Горшкова; используются задания для самостоятельной роботы по химии за 9 класс под редакцией Р. П. Суровцева, С. В. Софронова; используется сборник задач по химии для средней школы и для поступающих в вузы под редакцией Г. П. Хомченко, И. Г. Хомченко. В 9 классе на изучение данной темы отводится 4 ч.
Электролиз растворов
Электролизом называется окислительно-восстановительный процесс, протекающий на электродах при пропускании через электролит электрического тока. При электролизе катод является восстановителем, т. к. отдает электроны, а анод – окислителем, т. к. принимает электроны от анионов.
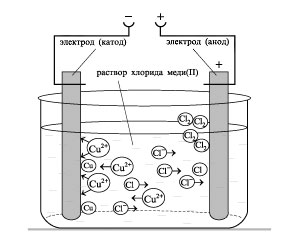
Электролиз раствора хлорида меди(II)
Для выбора наиболее вероятного процесса на катоде и аноде при электролизе растворов с использованием инертного (нерастворимого) анода (например, графита, угля, платины, иридия) используют следующие правила.
1. На аноде образуются:
а) при электролизе растворов, содержащих анионы F–, ![]() –,
–, ![]() ,
, ![]() , OH–, – O2;
, OH–, – O2;
б) при окислении анионов Сl–, Вr–, I– – соответственно Сl2, Вr2, I2.
2. На катоде образуются:
а) при электролизе растворов, содержащих ионы, расположенные в ряду напряжений левее Аl3+, – Н2;
б) если ионы расположены в ряду напряжений правее водорода – металлы; в) если ионы расположены в ряду напряжений между Аl3+ и H+, то на катоде могут протекать конкурирующие процессы – восстановление как металлов, так и водорода;
г) если водный раствор содержит катионы различных металлов, то их восстановление протекает в порядке уменьшения величины стандартного электродного потенциала (справа налево по ряду напряжений металлов).
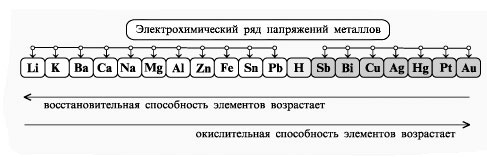
В случае использования активного (растворимого) анода (из меди, серебра, цинка, никеля, кадмия) анод сам подвергается окислению (растворяется) и на катоде кроме катионов металла соли и ионов водорода восстанавливаются катионы металла, полученные при растворении анода. Восстановительные свойства металлов удобно сравнивать, используя электрохимический ряд напряжений, в который включен и водород. Восстановительная способность элементов в этом ряду уменьшается слева направо, в этом же направлении увеличивается окислительная способность соответствующих катионов.
Электролиз расплавов электролитов
Рассмотрим электродные реакции на примере электролиза расплава хлорида натрия.
Под действием температуры ионная кристаллическая решетка NaCl разрушается на ионы Na+ и Cl-. Если погрузить в расплавленную соль два графитовых (инертных) электрода и подключить их к полюсам внешнего источника тока, то в электролите начнется направленное движение ионов и на электродах будут происходить следующие реакции:
Статьи о педагогике:
Петербургский воспитательный дом Дворец К.Г. Разумовского
2 (14) мая 1797 года император Павел I издал указ о передаче под покровительство императрицы Марии Федоровны и придании самостоятельного статуса Петербургскому воспитательному дому, открытому известным просветителем и педагогом И. И. Бецким. Воспитательный дом разместился в центре Санкт-Петербурга ...
Специфика ценностей российского общества
Многие ученые отмечают своеобразие исторического и социокультурного развития нашей страны, что связано не только с ее геополитическим положением, но и с культурой и менталитетом всего населения. Поэтому и смена ценностных идеалов у нас так же имеет свои индивидуальные черты. Как отмечают Лапин Н.И. ...
Пути повышения физической подготовленности учащихся на уроках
физической культуры
В организации занятий необходима цикличность развития физических качеств. На одном уроке развиваются выносливость и сила, на другом сила и быстрота, на третьем уроке выносливость, сила, быстрота. Гибкость и ловкость идут как «фоновые» физические качества, то есть они в различной степени развиваются ...
Меню
- Главная
- Воспитание трудолюбия дошкольников
- История развития педагогики
- Физическая культура в младших классах
- Детская и юношеская субкультуры
- Развитие женского образования в России
- Психология и педагогика
- Перспективы образования

